Periyodik sistemdeki elementler değişik şekillerde sınıflandırılmaktadır. Mesela, tabiatta bulunuş şekline göre tabii-suni olarak, metal-ametal özelliğine göre veya valens halkasındaki elektronların sayısı ve sistematiğine göre de ayrı bir sınıflandırma yapılmaktadır. Buna göre periyodik sistemdeki elementlerin sınıflandırması şu şekilde yapılabilir;
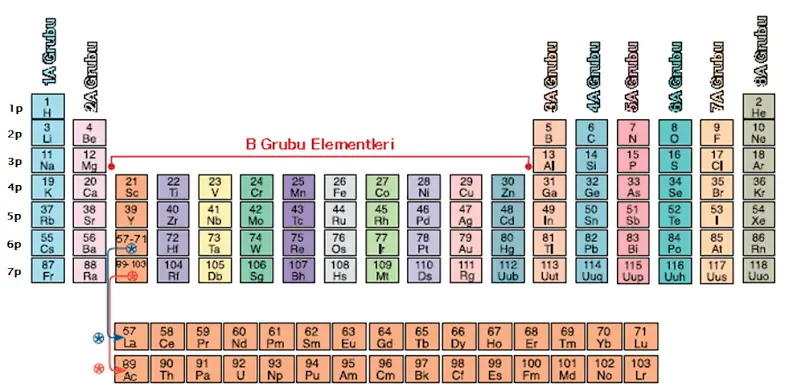
Esas Elementler
Tam dolu veya tamamen boş d-orbitaline sahip olup, valens elektronların (s) ve (p) orbitallerinde bulunduran elementlerdir. Hidrojen ve helyum elementlerinin valens elektronları ise sadece (s) orbitalinde bulunur. Her ne kadar bakır ve çinko grubu elementlerin de d-orbitalleri tamamen dolu ise de;
Bu son d-elektronlarını kimyasal bağ yapmada kullanabildikleri ve de kimyasal özellikleri bakımından daha çok geçiş elementlerine bezedikleri için, bu elementler geçiş elementleri grubuna dahil edilirler. Fakat çinko grubu elementler valens elektron sayıları aynı olduğu için, bazı özellikleri bakımından toprak alkali metallerine benzerler. Esas elemenler I A – VIII A arası sekiz gruptan oluşur.
Geçiş Elementler
Bu gruptaki elementlerin son iki halkaları kısmen doludur, diğer bir ifade ile; bunlar kısmen dolu d-orbitaline sahip elementlerdir. Kimyasal bağ oluşturma esnasında hem bu kısmen dolu d-elektronları, hem de en son halkadaki s-elektronlarını valens elektronu olarak kimyasal bağ yapımı için kullanılır. Bir periyot içerisinde bir elementten diğer bir elemente geçerken yeni gelen elektron kısmen dolu d-ortibaline yerleşir.
Geçiş elementleri III – II grupları arasında dört periyot halinde dizilen ve on gruptan oluşan 37 elementtir.
İç Geçiş Elementleri
Kısmen dolu 5. ve 6. halkaya (Lantanoidlerde) veya 6. ve 7. halkaya (Aktinoidlerde) sahip olan ve yeni gelen elektronları sondan üçücü halkaya yerleşen elementlere bu ad verilir. So iki halkalarındaki elektron sayıları bir kaç istisna dışında sabittir.
Bunlar periyodik sistemde lantan ve aktinyum elementlerini takip eden 14’er elementten meydana gelen iki periyot oluştururlar ve kendilerinden önce gelen iki elementte izafeten Lanta-noid ve Aktinoid şeklinde adlandırılırlar.
Soygazlar
Helyum hariç bütün soygazların valens elektron konfigurasyonları şeklindedir. Bu elektron konfigurasyonu çok kararlıdır ve bütün elementler buna ulaşmaya gayret ederler. Kararlı valens elektron konfigurasyonu;
- Yüksek iyonlaşma enerjisine sahip olmalarına,
- Reaksiyon yapma bakımından isteksiz olmalarına,
- Bu son nedenden dolayı da bunların tabiatta atomik halde bulunmalarına neden olmaktadır.
Periyodik sistemdeki elementlerin diğer sınıflandırması
Metaller
Bunlar elektriği iletirler ve metallerin karakteristik özelliklerini gösterirler. Esas, geçiş element ve iç geçiş elementler grubunda metaller bulunur. Sayıları şuan da 86’dır. Fakat yeni elementlerin sentez edilmesiyle bu sayı artmaktadır.
Yarı metaller
Esas elementler grubunda metallerle ametaller arasında yer alan B, Si, As, Se, Sb, Te ve At elementlerine yarı metal adı verilir. Çünkü bunlar fiziksel ve kimyasal özellik bakımından metaller ve ametaller arasında geçiş özelliği gösterirler. Bunların elektrik iletkenliği ısı ile artar ve kristal yapılarına yabancı elementlerin girmesiyle iletkenlik büyük ölçüde arttırılabilir.
Ametaller
Elektriği iletmeyen bu yalıtkan elementlere ametal adı verilir. Sayıları 16’dır. Metaller ve yarı metaller sadece katı oldukları halde (civa istisna) ametallerde gaz, sıvı ve katı olanları da vardır.
Elementler bir de tabiatta bulunşlarına göre sınıflandırılmaktadır. Tabiatlarına göre de sınıflandırmak gerekirse, şu şekilde sınıflandırabiliriz;
Tabii Elementler: Yer yüzündeki minerallerden, sudan ve havadan kazanılan elementlerdir. Sayıları şuan da 90 adettir.
Suni Elementler: Tabiatta şuanda kalmayan, ancak atom reaktörlerinde füzyon yolu ile elde edilen elementlerdir. Bunların dünyamızın başlangıcında var oldukları, ancak yarılanma sürelerinin kısa olması nedeniyle günümüze kadar ulaşamadığı kabul ediliyor. Bunların sayısı yeni elde edilen elementler nedeniyle devamlı değişmektedir. Suni elementlerin yarılanma süreleri kısa ve miktarları da az olduğu için paratik önemleri de sınırlıdır. Bunlar içerisinde kilo gram miktarında üretilen tek element teknesyumdır. Teknesyum, Tc ile ifade edilmektedir.
