Faz Diyagramı
Bir veya daha fazla sayıdaki madde ele alındığında maddenin gaz, sıvı veya katı özelliklerinden birini taşıdığı görülür. Katı (kristal) madde ise bir veya daha fazla değişik mineal madde olarak görülür. Sıvı madde de değişik bileşimli olarak birden fazla bileşim oluşturabilir. İşte bu fiziksel, bazen de hem fiziksel hemde kristal durumların her birine faz denir. Su normal basınçta 0 ºC’da hegzagonal sistem kristalleşir. Sıcaklık -120 ºC’ye düşürüldüğünde sistem kübik olur.
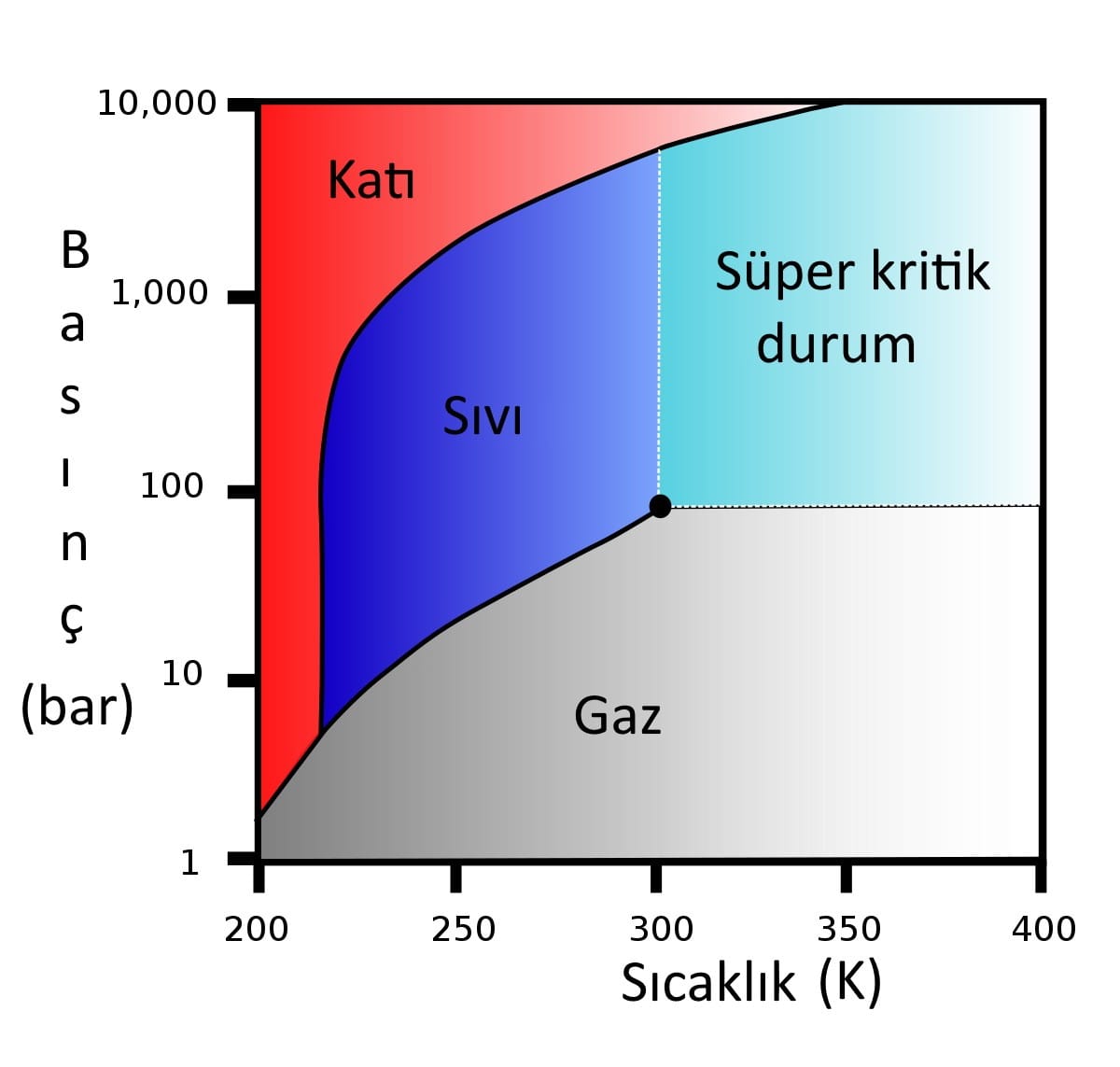
Burada, yani -120 ºC’de aynı bileşimli iki katı (kristal) faz söz konusunudur. Gaz fazı ise tektir, yani bileşim veya başka nedenler çok sayıda gaz fazın bir arada bulunmasına izin vermez.
Verilen su örneğinde su buharı, sıvı ve iki çeşit katı durumlarıyla birlikte sistem vardır. Yukarıdaki örnekte tek madde vardır. Bu tür sistemlere tek maddeli sistemler denir. Madde sayısı birden fazla olursa çok maddeli sistemler oluşur. Bir sistemi etkileyen faktörler; basınç, sıcaklık ve konsantrasyon (kimyasal bileşim)’dur. Bu sistemdeki bileşenler ve fazlar arasında şu bağıntı vardır.
(Gibbs Kuralı) S= B – F +2
S: Sistemin serbestlik derecesi
B: Bileşen sayısı
F: Faz sayısı
Yukarıdaki su sisteminde A noktasının durumu yukarıdaki formülde incelendiğinde bu noktanın basınç sıcaklık açısından sabit bir nokta olduğu görülür. Şöyle ki, A noktasında üç faz (katı, sıvı, gaz) dengede bulunmaktadır. Faz sayısı üçtür. Bileşenler ise sadece su olduğuna göre:
F: 3 B: 1
S= 1-3+2
S=0
Diyagramdaki B noktasında S=1-2+2‘dir. Bu demektir ki, basınç veya sıcaklıktan biri değiştiğinde bu iki faz (buhar ve sıvı) dengede kalır.
Bir Bileşimli Sistemler: Yukarıdaki su örneğinde olduğu gibi, bunlar bağımsız tek maddeden oluşan sistemlerdir. Bu sistemlere SiO2 tipik bir örnek olarak verilebilir.

İki Bileşenli Sistemler: A ve B gibi iki farklı maddeden oluşan eriyikler birbirleriyle karışmıyorsa, bunların katı (kristal) halleri de ayrı ayrı A ve B maddeleri şeklindedir. Bunların karışması durumunda ise kristal durumlarında çeşitli şıklar söz konusu olabilir. Bunlar;
1-) A ve B maddeleri sınırsız bir karışım kristal oluşturabilirler (sınırsız katı çözeltili ikili sistem)
2-) A ve B maddeleri kısmen karışım oluşturabilirler (sınırlı katı çözeltili ikili sistem)
3-) Karışım, kristal oluşmadan A ve B maddeleri yan yana kristalleşebilir (karışım kristalsiz ikili sistem)
4-) A ve B maddeleri kendi bileşimli kristallerinin yanı sıra başka bileşimli bir veya fazla bileşimli sayıda kristal faz oluşturabilir (ara bileşikli ikili sistem)
A ve B maddeleri elementler olabileceği gibi çok sayıda elementten oluşan bileşikler şeklinde de olabilir. (Na2O, K2O, FeO). Doğadaki maddeler genellikle bileşikler şeklindedir. İkili sistemleri kolay anlayabilmek için sistem parametrelerinin biri olan basınç sabit kabul edilir. Eğri üzerinde kristal oluşmaya başlar.
İki veya daha fazla maddeli sistemlerde bileşim bir parametre olarak eklenir. Sıcaklık düşey eksende, bileşim yatay eksende gösterilir.


Yorumlar kapalı, ancak trackbacks Ve pingback'ler açık.